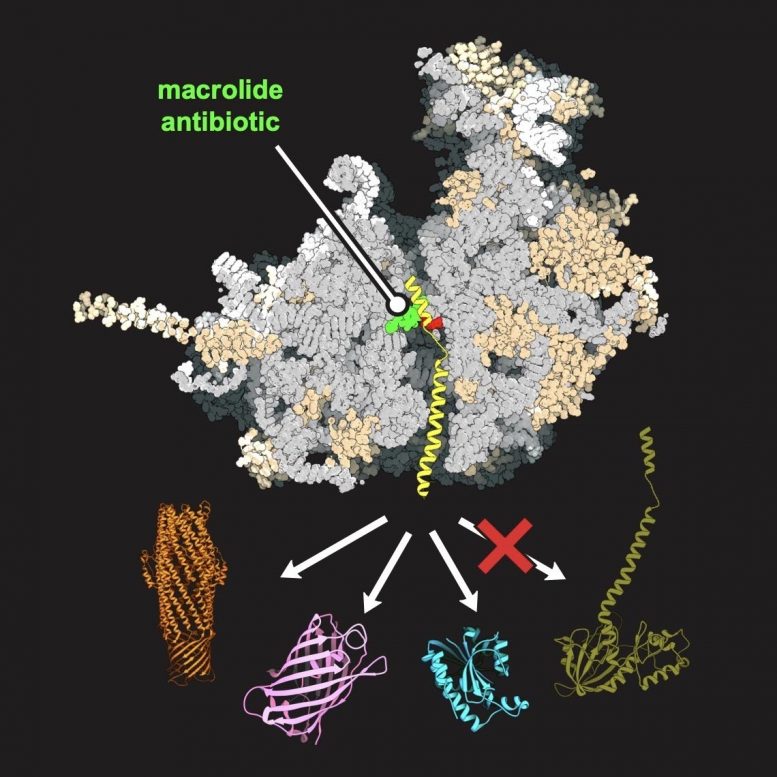
Das Antibiotikum (grün), das mit dem menschenähnlichen Hefe-Ribosom (grau) assoziiert ist, ermöglicht die Synthese einiger Proteine (dargestellt durch Orange, Lila und Blau), aber nicht anderer (dunkelgrün). Bildnachweis: Maxim Svetlov / UIC
UIC-Forscher haben nachgewiesen, dass für Bakterien entwickelte Medikamente das Potenzial haben, menschliche Zellen zu beeinflussen.
Laut Forschern der Universität von Illinois in Chicago können Antibiotika zur Behandlung häufiger bakterieller Infektionen wie Lungenentzündung und Sinusitis auch zur Behandlung menschlicher Krankheiten wie Krebs eingesetzt werden. Zumindest theoretisch.
Wie in der Datei gezeigt Naturkommunikation In der Studie zeigte das Team des UIC College of Pharmacy in Laborexperimenten, dass eukaryotische Ribosomen so modifiziert werden können, dass sie auf Antibiotika genauso reagieren wie prokaryotische Ribosomen.

Alexander Mankin ist Professor für medizinische und pharmakologische Chemie an der Alexander Nevach an der School of Pharmacy der University of California. Bildnachweis: UIC Photo Services / UIC
Pilze, Pflanzen und Tiere sind – wie Menschen – Eukaryoten. Es besteht aus Zellen, die einen klar definierten Kern haben. Andererseits sind Bakterien Prokaryoten. Es besteht aus Zellen, die keinen Kern haben und unterschiedliche Strukturen, Größen und Eigenschaften haben. Die Ribosomen von eukaryotischen und primitiven Zellen, die für die Proteinsynthese verantwortlich sind, die für das Zellwachstum und die Zellreproduktion notwendig ist, sind ebenfalls unterschiedlich.
„Einige Antibiotika, die zur Behandlung von bakteriellen Infektionen eingesetzt werden, wirken auf interessante Weise. Sie binden an das Ribosom von Bakterienzellen und hemmen selektiv die Proteinsynthese.“, Sagte Alexander Mankin, Professor für medizinische und pharmakokinetische Chemie am College of California der University of California Die Apotheke und leitende Autorin der Studie, Alexander Mankin. Einige Proteine herstellen, andere jedoch nicht. “Ohne diese Proteine würden die Bakterien sterben.
Wenn Menschen Antibiotika zur Behandlung von Infektionen verwenden, sind die Zellen des Patienten nicht betroffen, da die Medikamente nicht dafür ausgelegt sind, an Ribosomen verschiedener Formen eukaryotischer Zellen zu binden.
„Da es viele menschliche Krankheiten gibt, die durch die Expression unerwünschter Proteine verursacht werden – dies ist beispielsweise bei vielen Arten von Krebs oder neurodegenerativen Erkrankungen der Fall -, wollten wir wissen, ob ein Antibiotikum verwendet werden kann, um zu verhindern, dass die menschliche Zelle‚ nicht- Proteine ’Wünschenswerte, nur unerwünschte Proteine “, sagte Mankin.
Um diese Frage zu beantworten, untersuchten Mankin und der erste Studienautor Maxim Svetlov, ein Assistenzprofessor am Department of Pharmaceutical Sciences, Hefe, eine eukaryotische Zelle mit Zellen, die menschlichen Zellen ähneln.

Maxim Svetlov, wissenschaftlicher Mitarbeiter, Institut für Pharmazeutische Wissenschaften, Fakultät für Pharmazie, UIC. Bildnachweis: Svetlov / UIC
Mankin sagte, das Forschungsteam, dem Partner aus Deutschland und der Schweiz angehörten, habe einen „wunderbaren Trick“ gemacht. „Wir haben das Hefe-Ribosom so konzipiert, dass es Bakterien ähnlicher ist.“
Das Team von Mankin und Svetlov verwendete Biochemie und Mikrogenetik, um ein einzelnes Nukleotid von mehr als 7.000 im Hefe-Ribosom zu verändern. RNADies reichte aus, um ein Makrolid-Antibiotikum herzustellen – eine beliebte Klasse von Antibiotika, die durch Bindung an bakterielle Ribosomen wirken -, die auf das Hefe-Ribosom wirken. Mithilfe dieses Hefemodells verwendeten die Forscher Genomprofile und hochauflösende Strukturanalysen, um zu verstehen, wie jedes Protein in der Zelle synthetisiert wird und wie das Makrolid mit dem Hefe-Ribosom interagiert.
Mankin sagte: „Durch diese Analyse haben wir festgestellt, dass das Makrolid abhängig von der spezifischen Gensignatur des Proteins – dem Vorhandensein einer„ guten “oder„ schlechten “Sequenz – seine Produktion auf dem eukaryotischen Ribosom stoppen kann oder nicht.“ „Dies haben uns konzeptionell gezeigt, dass Antibiotika verwendet werden können, um die Proteinsynthese in menschlichen Zellen selektiv zu hemmen und um menschliche Störungen zu behandeln, die durch „schlechte“ Proteine verursacht werden.
Die Erfahrungen der UIC-Forscher bieten einen Ausgangspunkt für weitere Studien. „Jetzt, da wir wissen, dass die Konzepte funktionieren, können wir nach Antibiotika suchen, die in der Lage sind, unmodifizierte eukaryotische Ribosomen zu binden und sie zu verbessern, um nur die für den Menschen schädlichen Proteine zu hemmen“, sagte Mankin.
Referenz: „Kontextspezifische Wirkung von Makrolid-Antibiotika auf Eukaryoten-Ribosomen“ von Maxim S. Svetlov, Tim O. Koller, Sezin Maidan, Vaishnavi Shankar, Dorota Klipaki, Norbert Polasik, Nicholas R. Goedusch, Nora Vásquez-Lassib, Daniel N. Wilson und Alexander S. Mankin, 14. Mai 2021 Naturkommunikation.
DOI: 10.1038 / s41467-021-23068-1
Die beiden weiteren Co-Autoren der Studie sind Dorota Kalbaki und Nora Vasquez-Lassleb von der University of California. Tim Koller und Daniel Wilson von der Universität Hamburg; Medan und Nicholas Guidosh von den National Institutes of Health werden dekorieren; Norbert Polasik und Vishnavi Shankar aus Universität Bern.
Diese Arbeit wurde durch Zuschüsse der Nationalen Gesundheitsinstitute (R35 GM127134, DK075132, 1FI2GM137845), des Deutschen Forschungsfonds (WI3285 / 6-1) und des Schweizerischen Nationalfonds (31003A_166527) unterstützt.









More Stories
Die deutsche Luft- und Raumfahrtindustrie steht vor dem Ende des Typhoon-Programms
Airbus erhält 2,1 Milliarden Euro für den Aufbau eines deutschen militärischen Kommunikationssystems
RFA, ATMOS und Yuri kündigten den Mikrogravitationsdienst „Eva“ an